Impact of COPD on cardiopulmonary resuscitation in adults with in-hospital cardiac arrest
-
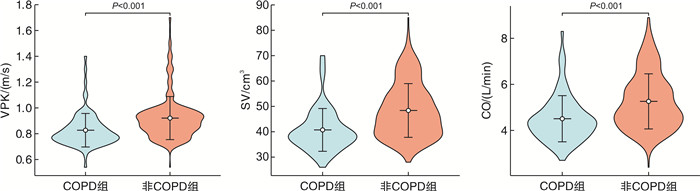
摘要: 目的 探讨合并慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)患者在院内心脏骤停的临床特征及其对心肺复苏的影响。方法 回顾性分析2020年9月-2024年4月在南昌大学第一附属医院急诊科接受治疗的院内心脏骤停患者407例,平均年龄为73岁,其中男性患者占81.8%;检索患者既往病史,根据是否合并COPD将其分为COPD组(88例,21.6%)和非COPD组(319例,78.4%)。两组患者均按照2020年国际心肺复苏和心血管急救指南进行急救。使用无创超声心输出量测定(ultrasonic cardiac output monitor,USCOM)监测两组患者在心肺复苏过程中的血流动力学变化,比较主动脉流动峰值速度(peak velocity of flow,VPK)、每搏心输出量(stroke volume,SV)、心输出量(cardiac output,CO)、自主循环恢复率、心肺复苏持续时间以及30 d出院生存率。结果 COPD组心肺复苏过程中的VPK、SV和CO均显著低于非COPD组,差异有统计学意义(P < 0.001)。COPD组的主循环恢复率及持续自主循环恢复>20 min的比例均低于非COPD组,两组差异有统计学意义(P < 0.05)。倾向性队列研究显示,COPD组的死亡率85.2%,而非COPD组的死亡率为72.1%,两组差异有统计学意义(P < 0.05),提示COPD与较高的死亡率相关。在可除颤心律和心肺复苏持续时间方面,两组患者之间差异无统计学意义(P>0.05)。多因素分析逻辑回归分析显示,合并COPD、心肺复苏持续时间过长和凝血功能障碍是自主循环恢复>20 min的危险因素,而体重指数是保护因素;心脏骤停年龄、合并COPD、心脏骤停类型(心搏停止和无脉性电活动)及肾衰竭是影响30 d出院生存的独立危险因素。结论 合并COPD的院内心脏骤停患者在徒手心肺复苏过程中表现出较低的心输出量,较低自主循环恢复率及较高的死亡率;在体重指数、初始可除颤心律及心肺复苏持续时间方面,两组患者差异无统计学意义;这些结果为更好地理解COPD患者在心肺复苏中的特点提供了重要的临床参考。
-
关键词:
- 慢性阻塞性肺疾病 /
- 心肺复苏 /
- 无创超声心输出量测定 /
- 院内心脏骤停
Abstract: Objective To explore the clinical characteristics of in-hospital cardiac arrest patients with chronic obstructive pulmonary disease(COPD) and their impact on cardiopulmonary resuscitation(CPR).Methods A retrospective analysis was conducted on in-hospital cardiac arrest patients treated in the Emergency Department of the First Affiliated Hospital of Nanchang University from September 2020 to April 2024. Patient histories were reviewed, and participants were divided into COPD and non-COPD groups. Both groups received CPR according to the 2020 International Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Non-invasive ultrasonic cardiac output monitoring(USCOM) was used to assess hemodynamic changes during CPR, comparing peak flow velocity(VPK), stroke volume(SV), cardiac output(CO), return of spontaneous circulation, the duration of CPR, and 30-day survival rates.Results A total of 407 patients were included, of which 88(21.6%) had COPD, with a mean age of 73 years and 81.8% being male. The VPK, SV, and CO during CPR in the COPD group were significantly lower than those in the non-COPD group, with statistical significance(P < 0.001). The ROSC rate and the proportion of sustained return of spontaneous circulation for more than 20 minutes in the COPD group were also lower than in the non-COPD group, with significant differences(P < 0.05). In the propensity score analysis, the mortality rate in the COPD group was 85.2%, compared to 72.1% in the non-COPD group, indicating a statistically significant difference(P < 0.05) and suggesting an association between COPD and higher mortality. There were no significant differences between the two groups regarding initial shockable rhythm and CPR duration(P>0.05). Multivariate logistic regression analysis showed that COPD, prolonged CPR duration, and coagulation dysfunction were risk factors for sustained return of spontaneous circulation exceeding 20 minutes, whereas body mass index was a protective factor. Age at cardiac arrest, presence of COPD, type of cardiac arrest(asystole or pulseless electrical activity), and renal failure were independent risk factors affecting 30-day survival.Conclusion Patients with in-hospital cardiac arrest and COPD exhibit lower cardiac output, reduced rates of return of spontaneous circulation, and higher mortality during CPR. However, there were no significant differences between the two groups concerning body mass index, initial shockable rhythm, and CPR duration. These findings provide important clinical insights for understanding the characteristics of COPD patients during cardiopulmonary resuscitation. -
-
表 1 两组院内心脏骤停患者临床特征比较
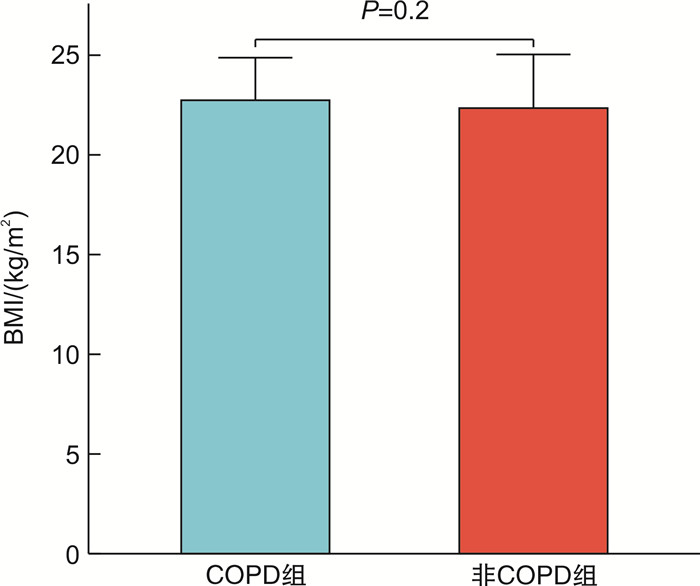
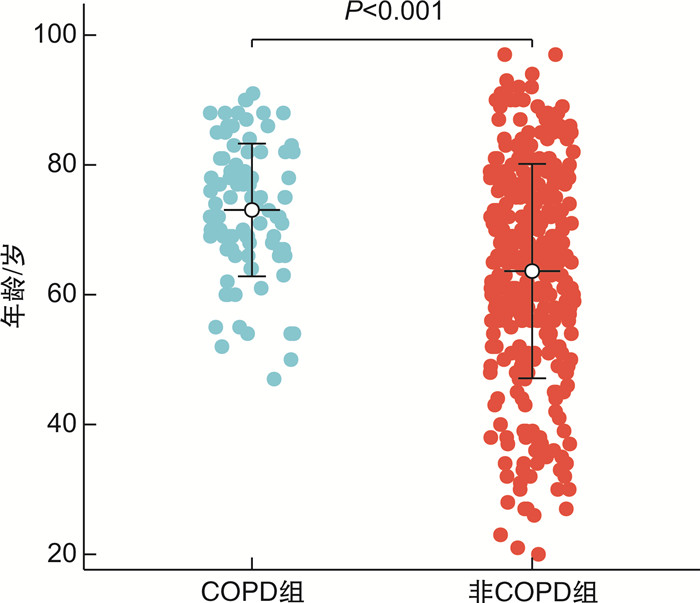
X±S,例(%) 指标 非COPD组(319例) COPD组(88例) P 年龄/岁 63.64±16.52 73.01±10.23 < 0.05 BMI/(kg/m2) 22.34±2.69 22.74±2.13 0.20 男性 214(67.1) 72(81.8) < 0.05 肾衰竭 109(34.2) 20(22.7) < 0.05 电解质紊乱 74(23.2) 32(36.4) < 0.05 冠心病/心力衰竭 117(36.7) 51(57.9) < 0.05 肝功能不全 52(16.3) 7(7.9) < 0.05 高血压病 98(30.7) 30(34.1) 0.50 糖尿病 52(16.3) 8(9.1) 0.09 贫血 124(38.9) 39(44.3) 0.35 脑梗死 39(12.2) 15(17.0) 0.20 凝血功能障碍 100(31.3) 21(23.9) 0.10 表 2 两组院内心脏骤停患者临床表现比较
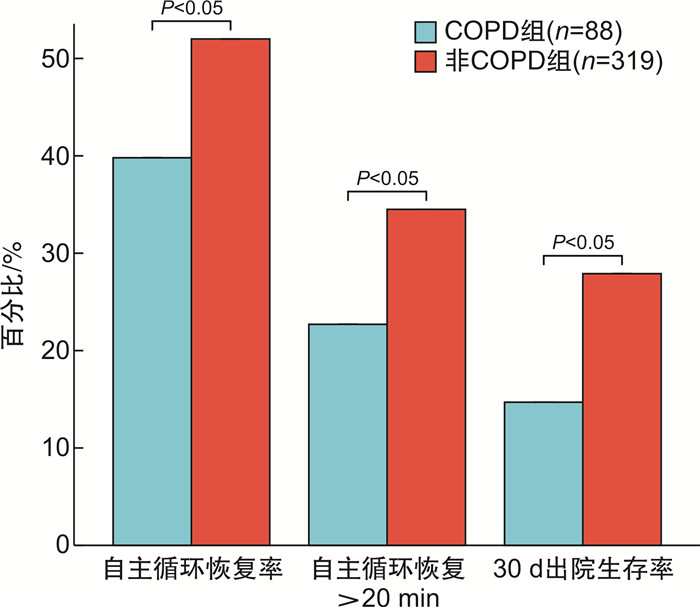
X±S,例(%) 指标 非COPD组(319例) COPD组(88例) P 初始节律/例(%) VF/VT 20(6.27) 5(5.68) 0.839 PEA/停止 299(93.7) 83(94.3) CPR时间/min 25.412±20.432 23.818±18.523 0.51 自主循环恢复率/例(%) 166(52.0) 35(39.8) < 0.05 自主循环恢复>20 min/例(%) 110(34.5) 20(22.7) < 0.05 30 d出院生存率/例(%) 89(27.9) 13(14.7) < 0.05 表 3 影响心脏骤停患者自主循环恢复>20 min多因素logistic回归分析
因素 B Wald χ2 OR 95%CI P 是否合并COPD 1.011 8.033 2.748 1.336~5.528 0.005 CPR持续时间 0.129 82.620 1.138 1.016~1.170 0.001 BMI -0.197 12.572 0.821 0.736~0.916 0.001 凝血功能障碍 0.961 8.542 5.585 1.178~5.799 0.018 常量 2.579 4.383 13.184 - 0.036 表 4 影响心脏骤停患者30 d出院生存率多因素logistic回归分析
因素 B Wald χ2 OR 95%CI P 年龄 0.29 7.423 0.011 1.008~1.051 0.006 是否合并COPD 0.878 5.024 0.392 1.117~5.186 0.025 心脏骤停类型 1.091 4.216 0.531 1.051~8.436 0.040 肾衰竭 0.954 8.542 0.326 1.369~4.924 0.003 常量 -3.271 2.128 2.242 - 0.145 -
[1] 王瑢. 中青年急性心肌梗死病人心搏骤停风险预测模型与验证[J]. 全科护理, 2024, 22(4): 764-767.
[2] 中国心脏骤停与心肺复苏报告编写组. 中国心脏骤停与心肺复苏报告(2022年版)概要[J]. 中国循环杂志, 2023, 38(10): 1005-1017.
[3] Christenson SA, Smith BM, Bafadhel M, et al. Chronic obstructive pulmonary disease[J]. Lancet, 2022, 399(10342): 2227-2242. doi: 10.1016/S0140-6736(22)00470-6
[4] 何雯青, 王佳佳, 谢洋, 等. 慢性阻塞性肺疾病疾病负担测评方法概述[J]. 中国卫生经济, 2024, 43(2): 58-61, 66.
[5] Kim N, Lee SH, Joe Y, et al. Effects of inhaled iloprost on lung mechanics and myocardial function during one-lung ventilation in chronic obstructive pulmonary disease patients combined with poor lung oxygenation[J]. Anesth Analg, 2020, 130(5): 1407-1414. doi: 10.1213/ANE.0000000000004733
[6] Mullin S, Lydon S, O'Connor P. The effect of operator position on the quality of chest compressions delivered in a simulated ambulance[J]. Prehosp Disaster Med, 2020, 35(1): 55-60. doi: 10.1017/S1049023X19005193
[7] Thomson RJ, Aung N, Sanghvi MM, et al. Variation in lung function and alterations in cardiac structure and function-Analysis of the UK Biobank cardiovascular magnetic resonance imaging substudy[J]. PLoS One, 2018, 13(3): e0194434. doi: 10.1371/journal.pone.0194434
[8] Yang JZ, Odish MF, Mathers H, et al. Outcomes of cardiopulmonary resuscitation in patients with pulmonary arterial hypertension[J]. Pulm Circ, 2022, 12(2): e12066. doi: 10.1002/pul2.12066
[9] Polman R, Hurst JR, Uysal OF, et al. Cardiovascular disease and risk in COPD: a state of the art review[J]. Expert Rev Cardiovasc Ther, 2024, 22(4-5): 177-191. doi: 10.1080/14779072.2024.2333786
[10] Lodge KM, Vassallo A, Liu B, et al. Hypoxia increases the potential for neutrophil-mediated endothelial damage in chronic obstructive pulmonary disease[J]. Am J Respir Crit Care Med, 2022, 205(8): 903-916. doi: 10.1164/rccm.202006-2467OC
[11] van den Berg ME, Stricker BH, Brusselle GG, et al. Chronic obstructive pulmonary disease and sudden cardiac death: a systematic review[J]. Trends Cardiovasc Med, 2016, 26(7): 606-613. doi: 10.1016/j.tcm.2016.04.001
[12] Khan MZ, Munir MB, Khan MU, et al. Sudden cardiac arrest in patients with chronic obstructive pulmonary disease: trends and outcomes from the national inpatient sample[J]. Am J Med Sci, 2022, 363(6): 502-510. doi: 10.1016/j.amjms.2021.10.025
[13] 陈亚红. 2020年GOLD慢性阻塞性肺疾病诊断、治疗及预防全球策略解读[J]. 中国医学前沿杂志(电子版), 2019, 11(12): 32-50.
[14] Merchant RM, Topjian AA, Panchal AR, et al. Part 1: executive summary: 2020 American heart association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care[J]. Circulation, 2020, 142(16_suppl_2): S337-S357.
[15] Sahu AK, Timilsina G, Mathew R, et al. "Six-dial strategy"-mechanical ventilation during cardiopulmonary resuscitation[J]. Indian J Crit Care Med, 2020, 24(6): 487-489. doi: 10.5005/jp-journals-10071-23464
[16] Yang IA, Jenkins CR, Salvi SS. Chronic obstructive pulmonary disease in never-smokers: risk factors, pathogenesis, and implications for prevention and treatment[J]. Lancet Respir Med, 2022, 10(5): 497-511. doi: 10.1016/S2213-2600(21)00506-3
[17] Adeloye D, Song PG, Zhu YJ, et al. Global, regional, and national prevalence of, and risk factors for, chronic obstructive pulmonary disease(COPD)in 2019: a systematic review and modelling analysis[J]. Lancet Respir Med, 2022, 10(5): 447-458. doi: 10.1016/S2213-2600(21)00511-7
[18] Konecny T, Somers KR, Park JY, et al. Chronic obstructive pulmonary disease as a risk factor for ventricular arrhythmias independent of left ventricular function[J]. Heart Rhythm, 2018, 15(6): 832-838. doi: 10.1016/j.hrthm.2017.09.042
[19] 中华医学会急诊医学分会, 中国老年医学学会急诊医学分会, 中国老年心肺复苏急诊专家共识组博, 等. 中国老年心肺复苏急诊专家共识[J]. 临床急诊杂志, 2024, 25(5): 213-220. https://lcjz.whuhzzs.com/article/doi/10.13201/j.issn.1009-5918.2024.05.001
[20] Yoo KH, Oh J, Lee H, et al. Comparison of heart proportions compressed by chest compressions between geriatric and nongeriatric patients using mathematical methods and chest computed tomography: a retrospective study[J]. Ann Geriatr Med Res, 2018, 22(3): 130-136.
[21] Janssens JP, Cantero C, Pasquina P, et al. Long-term noninvasive ventilation in chronic obstructive pulmonary disease: association between clinical phenotypes and survival[J]. Respiration, 2022, 101(10): 939-947.
[22] Miller AC, Wang X, Smith J. "Outcomes of cardiac arrest in patients with chronic obstructive pulmonary disease"[J]. J Card Fail, 2019, 25(6): 123-130.
[23] Saha BK, Bonnier A, Chong WH. Oxygen supplementation in COPD exacerbation with hypoxia and hypercapnia: what does the evidence show?[J]. South Med J, 2021, 114(9): 620-622.
[24] El-Chami MF, Garweg C, Iacopino S, et al. Leadless pacemaker implant, anticoagulation status, and outcomes: results from the Micra transcatheter pacing system post-approval registry[J]. Heart Rhythm, 2022, 19(2): 228-234.
[25] Matsumoto M, Tanaka Y, Suzuki T. "Impacts of COPD on cardiac function during resuscitation"[J]. Chest, 2021, 160(2): 123-130.
[26] McHugh EG, Grady ST, Collins CM, et al. Pulmonary, inflammatory, and oxidative effects of indoor nitrogen dioxide in patients with COPD[J]. Environ Epidemiol, 2023, 7(5): e271.
[27] González JD, Pérez R, López M. "Inflammatory markers and cardiac arrest outcomes in COPD patients"[J]. Am J Respir Crit Care Med, 2018, 197(8): 456-462.
[28] Zantah M, Dotan Y, Dass C, et al. Acute exacerbations of COPD versus IPF in patients with combined pulmonary fibrosis and emphysema[J]. Respir Res, 2020, 21(1): 164.
-



 下载:
下载: